研究内容
脂質ナノ粒子(LNP)の開発と核酸医薬を用いたがん治療への応用
●核酸医薬の実現に貢献する脂質ナノ粒子(LNP)
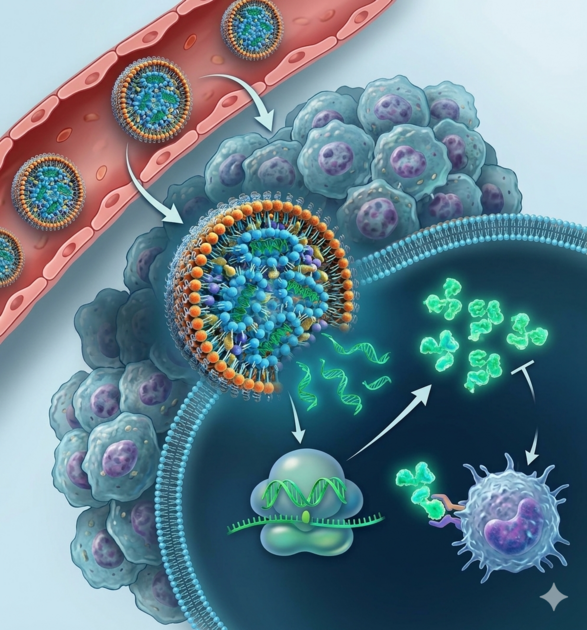
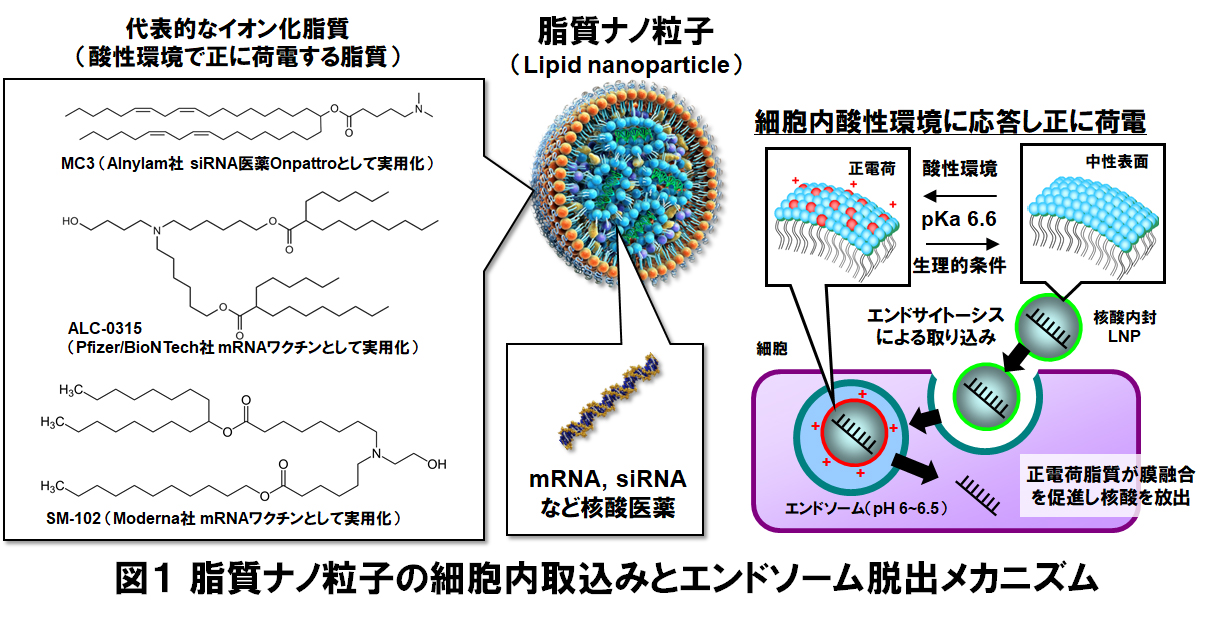
核酸医薬は新たな治療モダリティとして注目を集めています。核酸は負電荷を帯びた高分子であるため、疾患組織の標的細胞への導入にはドラッグデリバリーシステム(DDS)が必要不可欠です。これまでに承認されている核酸医薬には、脂質ナノ粒子(LNP)がDDSとして用いられています。イオン化脂質(pH応答性カチオン性脂質)はこの脂質ナノ粒子で最も重要な構成成分です。脂質ナノ粒子はエンドサイトーシスで細胞に取り込まれます。エンドソームのような酸性環境では、イオン化脂質はプロトンを受け取るため脂質ナノ粒子は正に荷電します。これにより脂質ナノ粒子はエンドソームと膜融合し、この過程で核酸医薬は細胞質へと到達します(図1)。このようなメカニズムで脂質ナノ粒子は核酸医薬の効率的な細胞内送達を実現しています。畠山は北海道大学薬学研究院の原島秀吉先生の研究室に在籍時より現在まで、新規のイオン化脂質の開発と脂質ナノ粒子による核酸医薬送達に関する研究を進めてきました(Sato Y, et al. J Control Release, 163, 267-276, 2012; Akita H, et al. Adv Healthc Mater, 2, 1120-1125, 2013; Sato Y, et al. Mol Ther, 24, 788-795, 2016; Maishi N, et al. Cancer Sci, 113, 1855-1867, 2022; Nakamura T, et al. J Control Release, 342, 200-213, 2022; Anindita J, et al. J Control Release, 289, 114414, 2026)。
●脂質ナノ粒子による核酸医薬の肝臓疾患への応用
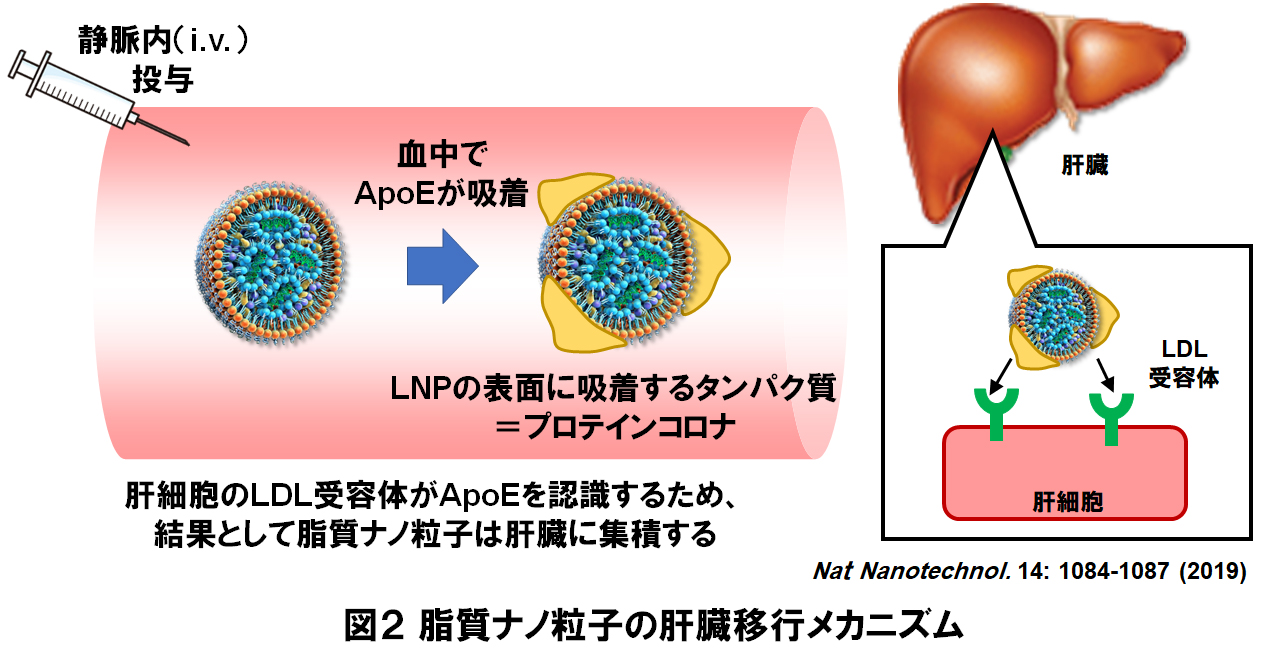
脂質ナノ粒子は静脈内投与すると、投与量の80~90%が肝臓に到達します。投与された脂質ナノ粒子は血液中で、ApoEが吸着します。ApoEは肝細胞のLDL受容体に認識されるため肝臓に効率的に集積することが分かっています。オンパットロはこの性質を利用することで、siRNAの肝臓への効率的な送達を実現し肝臓疾患に対象としたsiRNA医薬を実現しています。我々も独自のイオン化脂質による脂質ナノ粒子を用い肝臓への核酸医薬送達と肝炎など治療への応用についての成果を報告してきました(Takahashi M, et al. Nucleic Acids Res, 41, 10659-10667, 2013; Hatakeyama H, et al. J Control Release, 173, 43-50, 2014; Watanabe T, et al. Sci Rep, 4, 4750, 2014; Yamamoto N, et al. J Hepatol, 64, 547-555, 2016)。
一方で、肝臓以外の臓器や疾患部位への脂質ナノ粒子の送達、いわゆる「非肝臓デリバリー」が脂質ナノ粒子の今後の医薬への応用の課題となっています。
●非肝臓デリバリーの実現-腹膜播種への選択的送達を可能とする脂質ナノ粒子の開発
腹腔内の転移である腹膜播種は有効な治療法に乏しく、生存期間は短いのが現状です。新しい治療法の開発が望まれています。我々は、腹腔内投与が従来の静脈内投与に比べて抗体医薬の腹膜播種送達に有用であることを明らかとしました(Yamamoto M, et al. J Control Release, 352, 328-337, 2022)。脂質ナノ粒子についても同様で、腹腔内投与によって腹膜播種への送達量が静脈内投与の10倍以上増加しました。また、mRNA医薬を送達することで、非常に優れた治療効果を得ることに成功しています(特許出願準備中)。
さらに、イオン化脂質材料を検討することで、肝臓を回避し腹膜播種で選択的にmRNAが機能する脂質ナノ粒子を見出すことにも成功しました(特許出願準備中)。このように、適切な投与経路を選択することでmRNA医薬による腹膜播種の治療の可能性が示されています。送達メカニズムの解明を通じて、腹膜播種治療の実用化に向けた取り組みを行っています。