研究内容
免疫チェックポイント阻害剤の効き目を左右する体内動態要因の解明
●体内動態研究から探る免疫チェックポイント阻害剤のメカニズム
近年、免疫チェックポイント阻害剤やCAR-T細胞などのがん免疫療法が承認されています。がん免疫療法は従来では治療が困難であったがん治療が可能になり、劇的な薬効を示すことが報告されています。一方で、薬効を示す患者は20%程度であり、薬効を予測するマーカーや予測法の確立が課題です。免疫チェックポイント阻害剤は高分子の抗体医薬であり、投与されてから薬効や副作用発現に至る過程は従来の低分子化合物とは異なります。しかし、免疫チェックポイント阻害剤が投与されてからがん組織に到達までの体内動態に加え、がん組織内における分布など組織内動態がどのように薬効に影響するか解析はあまりなされていないのが現状です。複数の免疫チェックポイント阻害剤の感受性や耐性モデルにおける動態解析を通じて、動態のどのような要因が薬効に影響するか、臨床の課題に応えられる研究を進めています。
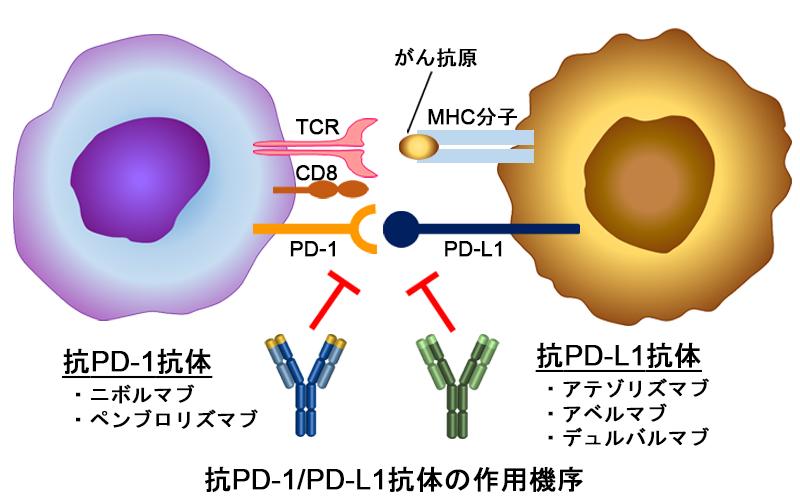
● 抗PD-1抗体と抗PD-L1抗体の体内動態の比較解析と薬効への影響
免疫チェックポイント阻害剤として現在、抗CTLA4抗体、抗PD-1抗体、抗PD-L1抗体で複数の薬剤が承認されています。特に抗PD-1/PD-L1抗体はがん治療の適応拡大が進んでいます。がん免疫療法では、がん細胞を排除するCD8陽性の細胞障害性T細胞の活性が重要です。PD-1は主にT細胞上に、PD-L1は主にがん細胞上に発現し、PD-1とPD-L1が結合することで、T細胞の活性が低下してしまうため、がん細胞は増殖が可能となります。この相互作用を阻害するのが抗PD-1抗体と抗PD-L1抗体です。両抗体はPD-1/PD-L1の同一経路を標的としています。では、この経路の阻害が有効ながんでは、どちらの抗体を投与しても同等の薬効が得られるのでしょうか?このような疑問に対する解答はありませんでした。
我々はPD-1/PD-L1阻害が有効な複数の担癌モデルマウスを用いて、両抗体の薬効と体内動態の比較解析を行いました。その結果、抗PD-L1抗体は体内動態の観点で、がんのみならず正常組織への分布と分解が多いため、抗PD-1抗体と比較して、がん組織への送達量が少なくなり、一部のがんでは抗PD-L1抗体の薬効が抗PD-1抗体に比べ劣ってしまうことを明らかとしました(Kurino T, et al. J ImmunoTher Cancer, 8, e000400, 2020)。従って、抗PD-L1抗体は正常組織への分布を飽和させるため高い投与量が必要となります。実際に臨床での投与量は抗PD-1抗体と比較し抗PD-L1抗体の方が約5倍高いですが、先の体内動態の違いが用量の差の一因と考えられます(日経産業新聞2019年6月18日に掲載)。その後、抗PD-1抗体と抗PD-L1抗体の臨床試験のメタ解析の結果、臨床においても抗PD-L1抗体と比較して抗PD-1抗体の薬効の優位性を示す報告がされました(Duan J, et al. JAMA Oncol, 6, 375-384, 2020)。我々の研究成果は、このような臨床の解析結果を裏付ける基礎研究からの知見と位置付けられます。
●Fc領域の性質が抗PD-L1抗体の薬効へ及ぼす影響
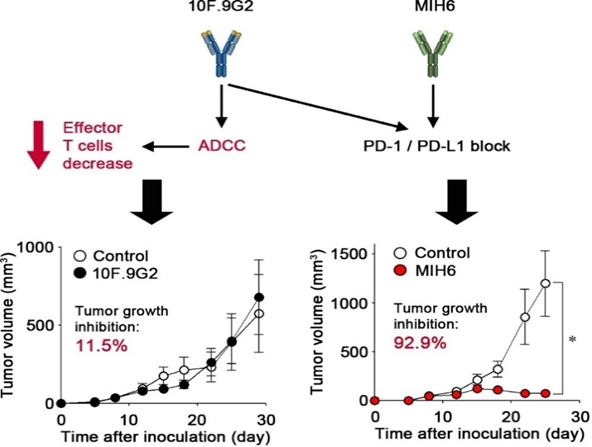
抗PD-L1抗体は、現在臨床で主に3剤(アテゾリズマブ、デュルバルマブ、アベルマブ)が承認されています。これら3剤のうちアベルマブはADCC活性が高い抗体です。同一分子PD-L1を標的とするこれら抗体薬剤の間に薬効などの差はないのでしょうか?我々は、マウスに対する抗PD-L1抗体でADCC活性の有無が薬効にどのように影響するか比較を行いました。その結果、ADCC活性の高い抗PD-L1抗体(10F.9G2)よりも、ADCC活性が低い抗PD-L1抗体(MIH6)の方が効果が優れていることが分かりました(下図)。一般的にはT細胞上にはPD-1が発現するとされていますが、PD-L1が発現することも報告されています。10F.9G2を投与したマウスでは、血液中のT細胞が減少していました。これは10F.9G2がADCC活性を介してT細胞の除去している可能性があります。このように、標的分子は同一でもFc領域の性質によって効果が異なることを報告しました(Tamemoto Y, et al. Int J Pharm, 679, 125755, 2025)。本成果は本学にてプレスリリースされました。https://www.cn.chiba-u.jp/en/news/press-release_e250724/
●データベースを用いた免疫関連有害事象(irAE)に関する解析
免疫チェックポイント阻害剤の副作用として、従来の医薬品とは異なる免疫関連有害事象(irAE)も臨床現場では問題となっています。免疫関連有害事象は、T細胞を活性化するという免疫チェックポイント阻害剤の作用に伴って発症するとされていますが、発症メカニズムも不明な点が多く残っています。副作用自発報告データベースを用いた解析を進めています。